在《科学报告》上发布的一项新研究中,Michael J. Rupar与美国佛罗里达州Hesperos公司的研究团队共同开发了一种高效的多器官无血清培养系统,旨在培养恶性疟原虫,这种原生动物是导致严重和致命疟疾的主要病因,从而为新药的研发提供创新平台。
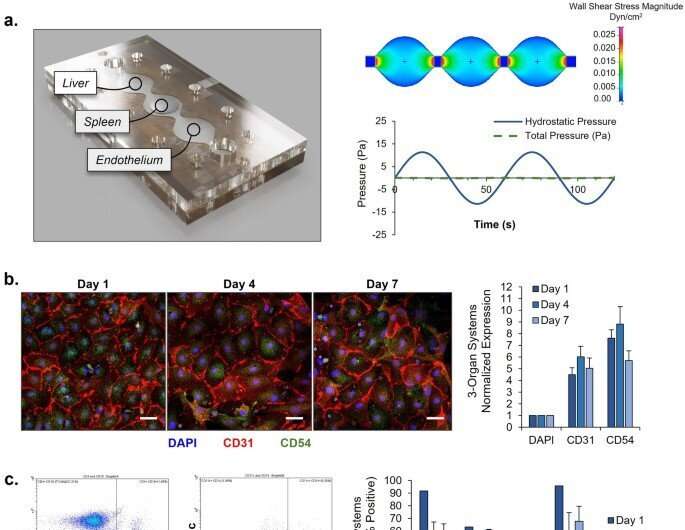
该系统包含四种人体器官模型,包括肝细胞、脾细胞、内皮细胞和循环血细胞,以模拟寄生虫感染的相互作用。研究团队使用了两种恶性疟原虫:3D7菌株对氯喹敏感,这是一种广泛使用的抗疟药物,而W2菌株则对氯喹具有耐药性。他们在循环微流体模型中维持了健康和病变状态下的功能细胞长达7天。
科学家们展示了一个有效的药物开发平台,在3D7菌株模型中,氯喹治疗显著降低了寄生虫血症。他们利用这一设置来确定治疗指数,并以剂量依赖的方式评估抗疟疾治疗的脱靶毒性。这些结果为在维持血液循环7天的真实人体模型中评估抗疟疾疗法开辟了新的途径。
恶性疟原虫的生命周期
本文来自作者[含巧]投稿,不代表万福山立场,如若转载,请注明出处:https://wak.ahwfs.cn/zheh/202505-504.html


评论列表(4条)
我是万福山的签约作者“含巧”!
希望本篇文章《构建人类疟疾芯片疾病模型》能对你有所帮助!
本站[万福山]内容主要涵盖:国足,欧洲杯,世界杯,篮球,欧冠,亚冠,英超,足球,综合体育
本文概览:...